Effetti collaterali del vaccino, è ufficiale. Cosa ha rilevato lo studio di Nature
Astratto
Attualmente in molti paesi sono in corso vaccinazioni su larga scala per il COVID-19 in risposta alla pandemia di COVID-19. Qui, riportiamo, oltre alla generazione di anticorpi neutralizzanti, alterazioni consistenti dell'emoglobina A1c, livelli sierici di sodio e potassio, profili di coagulazione e funzioni renali in volontari sani dopo la vaccinazione con un vaccino SARS-CoV-2 inattivato. Cambiamenti simili erano stati riportati anche nei pazienti COVID-19, suggerendo che la vaccinazione imitava un'infezione. Il sequenziamento dell'mRNA di una singola cellula (scRNA-seq) delle cellule mononucleate del sangue periferico (PBMC) prima e 28 giorni dopo la prima inoculazione ha anche rivelato alterazioni consistenti
nell'espressione genica di molti diversi tipi di cellule immunitarie. Riduzione di CD8 +Le cellule T e l'aumento del contenuto di monociti classici erano esemplari. Inoltre, scRNA-seq ha rivelato un aumento della segnalazione di NF-kB e una riduzione delle risposte all'interferone di tipo I, che sono state confermate da test biologici e si è verificato anche dopo l'infezione da SARS-CoV-2 con sintomi aggravanti. Nel complesso, il nostro studio raccomanda ulteriore cautela quando si vaccinano persone con condizioni cliniche preesistenti, tra cui diabete, squilibri elettrolitici, disfunzione renale e disturbi della coagulazione.introduzione
La pandemia di COVID-19 ha profondamente colpito l'umanità. Lo sviluppo di vaccini COVID-19 in varie forme è stato avviato in modo accelerato e senza precedenti. Nonostante alcune incertezze riguardo alle potenziali conseguenze, in molti paesi sono in corso vaccinazioni su larga scala. Sono stati sviluppati diversi vaccini COVID-19, tra cui particelle virali inattivate, vaccini mRNA, vaccini a base di adenovirali e così via. 1 , 2 , 3 , 4 , 5. Storicamente, la ricerca sui vaccini si è concentrata sul fatto che la vaccinazione potesse o meno generare anticorpi neutralizzanti per proteggere dalle infezioni virali, mentre le influenze a breve e lungo termine dei vari vaccini di nuova concezione sulla fisiopatologia umana e su altre prospettive del sistema immunitario umano non hanno stato completamente studiato.
Con lo sviluppo della tecnologia di sequenziamento dell'mRNA a cellula singola su larga scala (scRNA-seq), è diventato possibile un'indagine sistematica con precisione della funzione del sistema immunitario delle persone, principalmente attraverso l'scRNA-seq delle cellule mononucleate del sangue periferico (PBMC). Durante la pandemia di COVID-19, un ampio corpo di studi utilizzando scRNA-seq di PBMC aveva rivelato cambiamenti dettagliati nell'espressione genica in diversi sottotipi di cellule immunitarie, inclusi diversi tipi di cellule T e B, cellule NK, monociti, cellule dendritiche, ecc. durante e dopo l'infezione, i risultati da cui hanno indicato CD4 + e CD8 + . notevolmente ridottiNumeri di cellule T ed esaurimento delle cellule T in caso di infezione da SARS-CoV-2. È stata osservata anche una riduzione del numero di cellule T invariabili associate alla mucosa periferica (MAIT) e la loro migrazione dentro e fuori il polmone. Risposte immunitarie infiammatorie altamente attivate, tra cui risposte interferone-gamma (IFN-γ), interleuchina-6 (IL-6) e NF-κB, sono state riportate in pazienti COVID-19 6 , 7 , 8 , 9 , 10 , 11 , 12. Molti studi avevano rivelato differenze di stato immunitario tra le persone con sintomi gravi rispetto a quelli lievi, in quanto le forti risposte all'interferone di tipo I (IFN-α/β) erano benefiche dopo l'infezione da COVID-19 e le risposte attenuate all'IFN-α/β erano associate allo sviluppo di sintomi gravi 13 . Al contrario, risposte infiammatorie NF-kB più forti sono state associate a sintomi più gravi 14 . Inoltre, è stato riportato che l'aumento delle cellule γδ-T e la riduzione del contenuto di neutrofili sono associati a sintomi più lievi 15 .
In seguito alle infezioni da SARS-CoV-2, molte persone hanno sviluppato vari gradi di sindromi respiratorie e alcune con condizioni gastrointestinali. Era stato riferito che disturbi della coagulazione del sangue, problemi di vascolarizzazione, elettroliti squilibri, disturbi renali, disturbi metabolici, ecc sono stati grandi complicazioni cliniche con COVID-19 16 , 17 . Il modo in cui la vaccinazione mimerebbe un'infezione non è stato completamente valutato. In questo studio, abbiamo arruolato volontari sani che dovevano essere vaccinati con un vaccino SARS-CoV-2 inattivato (Vero Cell) 3, per partecipare ai test sugli anticorpi e sugli anticorpi neutralizzanti, nonché sulle misurazioni cliniche dettagliate di laboratorio prima e in momenti diversi dopo la vaccinazione (sono stati applicati regimi a due dosi con schemi leggermente diversi). Con nostra sorpresa, abbiamo osservato cambiamenti fisiopatologici abbastanza consistenti per quanto riguarda il contenuto di elettroliti, i profili di coagulazione, la funzione renale e le caratteristiche metaboliche del colesterolo e del glucosio, come se queste persone avessero avuto un'infezione da SARS-CoV-2. Inoltre, i risultati di scRNA-seq delle PBMC hanno indicato anche riduzioni consistenti di CD8 +Cellule T e aumenti del contenuto di monociti, nonché una maggiore segnalazione infiammatoria di NF-kB, che imitava anche le risposte dopo l'infezione. Sorprendentemente, le risposte all'interferone di tipo I, che erano state collegate a danni ridotti dopo l'infezione da SARS-CoV-2 e sintomi più lievi, sembravano essere ridotte dopo la vaccinazione, almeno di 28 giorni dopo la prima vaccinazione. Ciò potrebbe suggerire che nel breve termine (1 mese) dopo la vaccinazione, il sistema immunitario di una persona si trova in uno stato non privilegiato e potrebbe richiedere maggiore protezione.
Risultati
Follow-up longitudinale della produzione di anticorpi anti-SARS-CoV-2 e di anticorpi neutralizzanti dopo l'inoculazione del vaccino SARS-CoV-2 inattivato
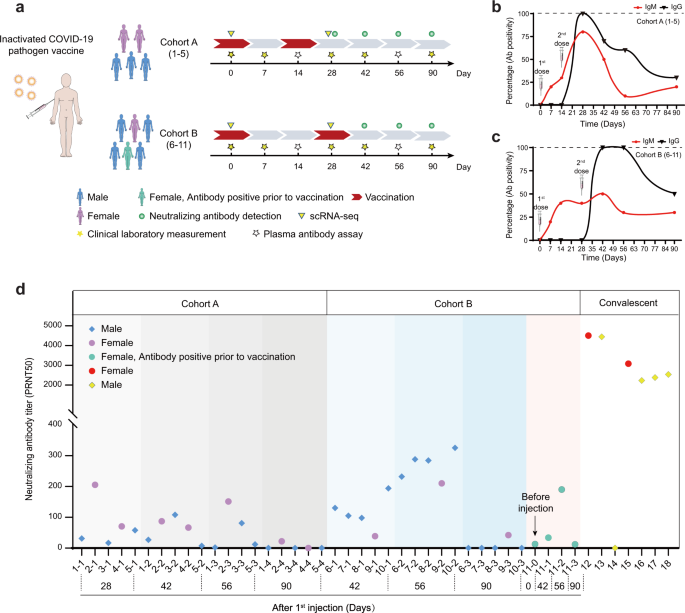
In questo studio sono stati arruolati un totale di 11 volontari adulti sani di entrambi i sessi, di età compresa tra 24 e 47 anni, con un BMI di 21,5-30,0 kg/m² (Fig. 1a e tabelle supplementari S1 e S2 ). Il vaccino SARS-CoV-2 (Vero Cell), inattivato (Beijing Institute of Biological Products Co. Ltd), è stato somministrato per via intramuscolare nel deltoide. I volontari sono stati divisi in due coorti; cinque partecipanti (coorte A) sono stati vaccinati con una dose intera (4 µg) di vaccino SARS-CoV-2 inattivato (cellule Vero) nei giorni 1 e 14 e sei partecipanti (coorte B) hanno ricevuto una dose completa del vaccino nei giorni 1 e 28 (Fig. 1a). Uno dei volontari del gruppo B è risultato positivo per anti-SARS-CoV-2 IgM e IgG subito prima della vaccinazione, indicativo di potenziali infezioni precedenti. Tuttavia, non vi era alcuna registrazione di precedenti positività mediante diagnosi di acido nucleico (NA) per COVID-19 (contrassegnato in verde in Fig. 1a ). Per tutti gli esami di follow-up, i dati di questo individuo sono stati contrassegnati in verde per tenere traccia di eventuali influenze da potenziali infezioni precedenti.
a Descrizione schematica delle strategie di inoculazione dei vaccini, raccolte di campioni di sangue e misurazioni. b , c Variazioni della positività anticorpale (percentuale positiva/totale) nel tempo nelle coorti A e B. I volontari della coorte A sono stati inoculati nei giorni 1 e 14 e nella coorte B nei giorni 1 e 28. La linea rossa rappresenta i cambiamenti di IgM e nero, IgG. d Cambiamenti del titolo anticorpale neutralizzante nel plasma di volontari nelle coorti A e B dopo la vaccinazione, nonché in quelli di soggetti convalescenti testati.
Gli eventi avversi sono stati monitorati quotidianamente durante i primi 7 giorni dopo ogni vaccinazione e poi autoregistrati dai partecipanti su schede diario nelle settimane successive. Nel complesso, le reazioni avverse sono state lievi (grado 1 o 2) e transitorie (Tabella supplementare S3 ). I campioni di sangue sono stati raccolti nei giorni 0, 7, 14, 28, 42, 56 e 90 e i campioni di urina sono stati raccolti nei giorni 0, 14, 28, 42 e 90. I campioni di plasma sono stati sottoposti a anti-SARS-CoV- 2 test IgM/IgG utilizzando più kit diagnostici, per la quantificazione sono stati utilizzati i risultati del kit più sensibile (Fig. 1b, c). I risultati dei test della coorte A hanno dimostrato che prima della seconda inoculazione lo 0% dei partecipanti ha sviluppato IgG anti-SARS-CoV-2, ma entro il giorno 28, ovvero 2 settimane dopo la seconda inoculazione, il 100% dei partecipanti è risultato positivo ( Fig. 1b ). Nel complesso, le IgM si sono presentate prima delle IgG, come previsto. La positività di IgG e IgM è diminuita entro il giorno 42 ed è rimasta a livelli relativamente bassi entro il giorno 90 nella coorte A. Per la coorte B, nessuno ha sviluppato IgG fino a dopo la 2a inoculazione. Tuttavia, al giorno 42, la positività delle IgG ha raggiunto il 100% (Fig. 1c) e mantenuto fino al giorno 56, suggerendo che il protocollo di vaccinazione per la coorte B era più efficace. Al giorno 90, anche la positività delle IgG si è ridotta al 50%, indicando che la produzione di anticorpi non si è mantenuta per molto tempo. Abbiamo inoltre effettuato test per gli anticorpi neutralizzanti SARS-CoV-2 18 (Fig. 1d ) e i risultati hanno anche indicato che due inoculazioni a distanza di 28 giorni (coorte B) hanno determinato titoli anticorpali protettivi più elevati rispetto a due inoculazioni a distanza di 14 giorni ( coorte A). D'altra parte, è apparso che i titoli anticorpali neutralizzanti anti-SARS-CoV-2 erano complessivamente inferiori a quelli degli individui convalescenti COVID-19 come riportato prima del 3 (Fig. 1d) .). Entro 90 giorni, i titoli anticorpali neutralizzanti sono diminuiti drasticamente in tutti i volontari (Fig. 1d ). È interessante notare che l'individuo che era positivo agli anticorpi prima della vaccinazione non era più incline a generare anticorpi neutralizzanti rispetto al resto dei partecipanti, suggerendo che la precedente potenziale infezione potrebbe non essersi verificata o potrebbe non generare una protezione di lunga durata nella prospettiva della neutralizzazione produzione di anticorpi.
Alterazioni nelle misurazioni di laboratorio clinico dopo la vaccinazione
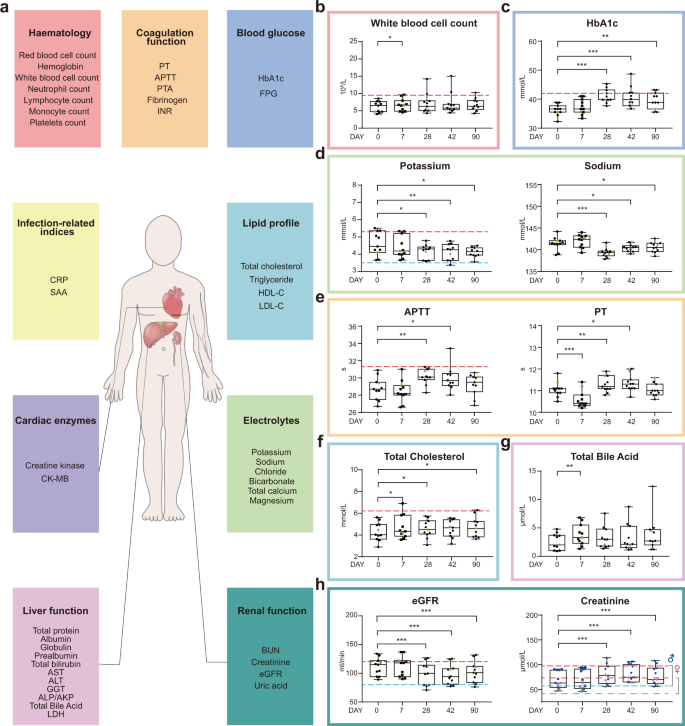
Sono stati misurati test di routine di laboratorio clinico, inclusi indici correlati alle infezioni, parametri ematologici, funzione della coagulazione, glicemia, lipidi sierici, enzimi correlati alla funzione cardiaca, elettroliti, biomarcatori correlati alla funzione epatica e renale, per rivelare le caratteristiche di sicurezza del vaccino (Fig. . 2a e tabelle supplementari S4 e S5 ). La conta dei globuli bianchi era significativamente, ma solo leggermente, aumentata dopo la vaccinazione il giorno 7. Nessuna differenza era rilevabile nei seguenti momenti (Fig. 2b). Con nostra sorpresa, sono stati osservati aumenti abbastanza consistenti dei livelli di HbA1c in volontari sani, indipendentemente dal fatto che appartenessero alla coorte A o B. Entro il giorno 28 dopo la prima inoculazione, tre individui su 11 hanno raggiunto il range prediabetico (Fig. 2c ). Entro i giorni 42 e 90, i livelli medi di HbA1c sembravano tornare indietro, ma erano ancora significativamente più alti di quelli prima della vaccinazione. Lavori precedenti hanno dimostrato che i pazienti diabetici con livelli di glucosio nel sangue incontrollati sono più inclini a sviluppare forme gravi di COVID-19 19 . È stato dimostrato che alti livelli di glucosio nel sangue/glicolisi promuovono la replicazione di SARS-CoV-2 nei monociti umani attraverso la produzione di specie reattive dell'ossigeno mitocondriale e l'attivazione di HIF1A 20, presentando quindi una caratteristica svantaggiosa.
a I test di routine di laboratorio clinico includono parametri ematologici e della coagulazione, indici relativi alla glicemia e alle infezioni, profilo lipidico, enzimi cardiaci, elettroliti, biomarcatori correlati alla funzionalità epatica e renale. Maggiori informazioni possono essere trovate nelle Tabelle Supplementari S4 e S5 . Valori dei test di laboratorio di conta leucocitaria ( b ), HbA1c ( c ), potassio ( d , pannello sinistro), sodio ( d , pannello destro), APTT ( e , pannello sinistro), PT ( e , pannello destro), totale colesterolo ( f ), acido biliare totale ( g ), eGFR ( h , pannello sinistro), creatinina ( h, pannello di destra). I punti dati rappresentano i valori di ogni individuo. I grafici a scatola hanno mostrato il 25°, 50° (mediana) e 75° percentile. Le linee tratteggiate orizzontali hanno mostrato i limiti normali superiori (rosso) in b , c , d (pannello sinistro), e (pannello sinistro), f , h e i limiti normali inferiori (blu) in d (pannello sinistro) e h . I valori di P sono stati calcolati mediante il test del rango del segno di Wilcoxon confrontando le misurazioni di laboratorio di volta in volta con le misurazioni di base. * P 0,05, ** P 0,01, *** P 0,001.
I livelli sierici di potassio sono diminuiti significativamente nei giorni 28, 42 e 90 dopo la prima inoculazione, con un campione al di sotto del limite normale inferiore al giorno 42 (Fig. 2d , pannello di sinistra). Allo stesso modo, anche i livelli sierici di sodio sono diminuiti dopo la vaccinazione (Fig. 2d , pannello di destra), indicativo dell'influenza del vaccino sull'equilibrio elettrolitico. Anche in questo caso, lo squilibrio elettrolitico è stato collegato anche al COVID-19 21 . La coagulopatia è un'altra condizione clinica indotta da COVID-19 22. Abbiamo scoperto che i profili di coagulazione cambiavano significativamente dopo la vaccinazione, a breve termine (7 giorni) dopo la prima inoculazione, i profili di coagulazione tendevano a un tempo di protrombina (PT) più breve, mentre l'effetto a lungo termine (28 e 42 giorni) era verso tempo di tromboplastina parziale attivato (APTT) e prolungamento del tempo di protrombina (Fig. 2e ). Al giorno 90, i profili sono tornati a quelli prima della vaccinazione (Fig. 2e ). Inoltre, abbiamo riscontrato livelli elevati di colesterolo nel sangue ai giorni 7, 28 dopo la prima inoculazione e livelli elevati di acidi biliari totali sono stati rilevati anche al giorno 7 (Fig. 2f, g). La disfunzione renale è un'altra condizione clinica legata al COVID-19 e, 28, 42 e 90 giorni dopo la prima inoculazione, i livelli di creatinina sierica erano significativamente più alti di quelli prima della vaccinazione, con conseguente riduzione dell'eGFR (Fig. 2h ). È stato riportato che la maggior parte di queste caratteristiche cliniche è associata allo sviluppo di sintomi gravi nei pazienti COVID-19 (Tabella supplementare S6 ). Nel complesso, non ci sono state differenze statisticamente significative tra le coorti A e B, ad eccezione di pochi indici (Tabella supplementare S7 ), pertanto i dati di due coorti sono stati raggruppati per la presentazione dei dati clinici e le successive analisi.
scRNA-seq ha rivelato alterazioni drammatiche nell'espressione genica di quasi tutte le cellule immunitarie dopo la vaccinazione
Per esplorare le caratteristiche immunologiche dei volontari sani dopo la vaccinazione, abbiamo eseguito scRNA-seq (10× Genomics) basato su goccioline per studiare i profili trascrittomici delle PBMC da volontari appartenenti alla coorte A o B, prima e 28 giorni dopo la vaccinazione (Fig. 3a e Fig. S1a supplementare ). Dopo la preelaborazione e l'eliminazione delle cellule di bassa qualità (vedi "Materiali e metodi"), abbiamo ottenuto 188.886 cellule da tutti i campioni PBMC, tra cui 86.685 cellule della coorte A e 102.201 cellule della coorte B. Tutte le cellule qualificate sono state integrate nel set di dati unificato e sottoposto ad analisi a valle.
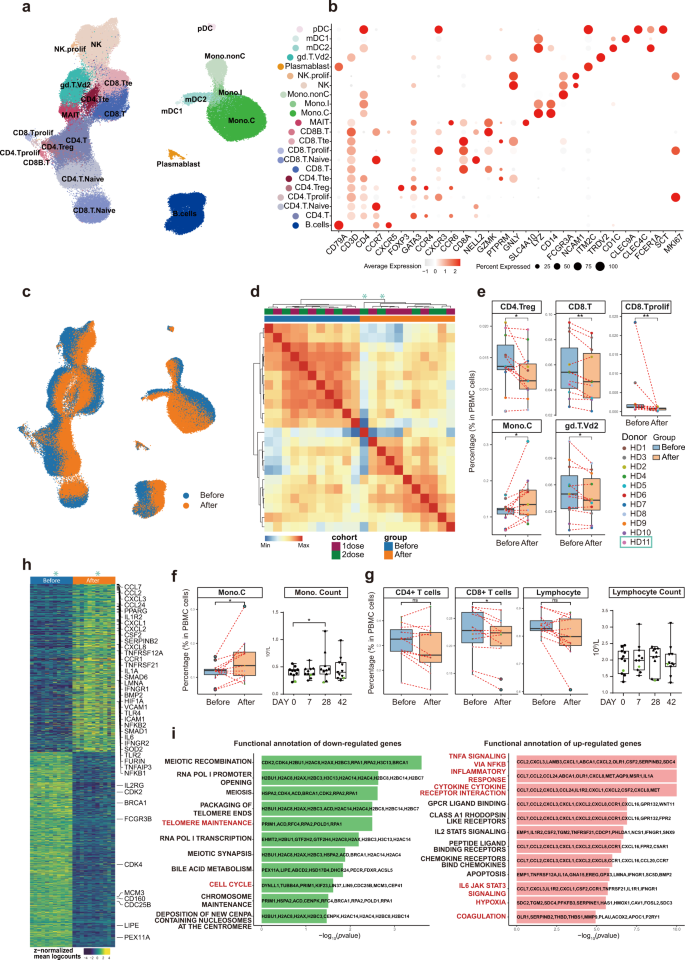
una rappresentazione UMAP di tipo cellulare di tutti i campioni uniti. In totale, 22 tipi di cellule sono stati identificati da firme di espressione genica specifiche per tipo di cellula. In totale, sono state rappresentate 188.886 cellule. b Dot plot per geni signature specifici del tipo di cellula. La scala di colori indicava i livelli di espressione e la dimensione in punti rappresentava la percentuale di cellule per cluster/sottotipo che esprimevano il gene corrispondente. c Rappresentazione UMAP che rappresenta le cellule prima (blu) e dopo la vaccinazione (arancione). d Heatmap di correlazione tra campioni pseudo-bulk. ePercentuali di specifici sottotipi di cellule immunitarie nei PBMC totali di ciascun individuo prima e dopo la vaccinazione. Il box plot rappresentava la distribuzione del campione. I riquadri blu rappresentavano i campioni prima e quelli arancioni dopo la vaccinazione. I valori di P erano basati sul test di Wilcoxon per i confronti tra i gruppi prima e dopo la vaccinazione. f I box plot hanno mostrato cambiamenti prima e dopo la vaccinazione nel contenuto di monociti dai dati scRNA-seq (pannello di sinistra) e misure di laboratorio clinico (pannello di destra). g I box plot hanno mostrato cambiamenti nel contenuto dei linfociti CD4 + , CD8 + e dei linfociti (T + B + NK) prima e dopo la vaccinazione dai dati scRNA-seq (pannelli 3 a sinistra) e dai test di laboratorio (pannello a destra). hDEG identificati da campioni pseudo-bulk prima e dopo la vaccinazione. i Analisi della sovrarappresentazione dei set di geni HALLMARK da MSigDB che dimostrano diverse caratteristiche immunologiche prima e dopo la vaccinazione.
Utilizzando il clustering basato su grafici dell'approssimazione e della proiezione del collettore uniforme (UMAP) 23 , l'algoritmo Single-cell Recognition of cell types (SingleR) 24 e l'annotazione manuale basata su marcatori di geni canonici, abbiamo identificato 22 tipi o sottotipi di cellule ed eseguito analisi dell'espressione differenziale tra tutti i tipi di cellule (Fig. 3b e Tabella supplementare S8 ). Le cellule (trascrittomi cellulari) dei campioni prima (blu) e dopo la vaccinazione (arancione) erano nettamente separate nella rappresentazione UMAP per entrambe le coorti, il che significava che le caratteristiche immunologiche erano cambiate in modo abbastanza drastico in quasi tutti i tipi di cellule immunitarie rilevate e in modo coerente in tutti i volontari ( Fig. 3c). Tra le 11 coppie (prima e dopo) di campioni PBMC, 10 coppie sono state sequenziate insieme e una coppia è stata sequenziata separatamente in un lotto diverso. Le distribuzioni UMAP erano drasticamente simili indipendentemente dai diversi lotti, suggerendo effetti batch di sequenziamento minimi (Figura complementare S1b ). Due lotti indipendenti di sequenziamento hanno rivelato cambiamenti simili prima e dopo la vaccinazione, suggerendo che i cambiamenti sono reali, mentre utilizzando il metodo di correzione dell'effetto batch (Harmony 25 ) (Figura supplementare S1c–e) comporterebbe una filtrazione eccessiva e l'eliminazione dei cambiamenti reali causati dalla vaccinazione. Inoltre, il raggruppamento dei campioni basato sul coefficiente di correlazione di Pearson dei trascrittomi indicava che i campioni delle due coorti (A e B) si mescolavano bene tra loro sia prima che dopo la vaccinazione, mentre i cambiamenti indotti dalla vaccinazione potevano essere chiaramente osservati (Fig. 3d ). . Pertanto, per aumentare la potenza statistica, abbiamo combinato le due coorti per analisi successive.
Per rivelare le differenze nelle composizioni dei tipi cellulari prima e dopo la vaccinazione, abbiamo calcolato le percentuali relative di tutti i tipi di cellule nelle PBMC di ciascun individuo sulla base dei dati scRNA-seq (Fig. 3e ). Abbiamo osservato diminuzioni del contenuto di cellule T regolatorie CD4 + (CD4.Treg), cellule T CD8 + (CD8.T) e cellule CD8 + proliferanti (CD8.Tprolif) dopo la vaccinazione (Fig. 3e ). Anche le diminuzioni dei contenuti delle cellule γδ-T (gd.T.Vd2) sono state significative (Fig. 3e ). Al contrario, la vaccinazione ha aumentato il contenuto di CD14 + monociti classici (Mono.C) (Fig. 3e ), coerentemente con le misurazioni di laboratorio clinico (Fig. 3f). Il contenuto complessivo dei linfociti, che includeva tutte le cellule CD4 + T, tutte le cellule CD8 + T, le cellule B e le cellule NK, non è cambiato significativamente prima e dopo la vaccinazione, il che è stato confermato anche da misurazioni di laboratorio clinico (Fig. 3g ). Abbiamo raccolto un set di dati pubblicato da 196 pazienti e controlli infetti da COVID-19 7 e abbiamo analizzato i nostri dati insieme a quel set di dati. Il risultato ha indicato che anche i cambiamenti indotti dalla vaccinazione nel contenuto cellulare di tutti e cinque i diversi sottotipi di cellule immunitarie sono cambiati nelle stesse direzioni nei pazienti COVID-19 rispetto ai controlli, ad eccezione delle cellule T CD8 + proliferanti (Figura complementare S2 ).
Per studiare i cambiamenti dettagliati dell'espressione genica indotti dalla vaccinazione, abbiamo unito campioni individuali in campioni pseudo-bulk e utilizzato test di campioni accoppiati per identificare i geni differenzialmente espressi (DEG) (Fig. 3h e Tabella supplementare S9 ). Geni significativamente sovraregolati erano coinvolti nella "segnalazione TNFα tramite NF-κB", "risposte infiammatorie" e "interazione recettore citochina-citochina", "segnalazione IL6-JAK STAT3", "coagulazione", "ipossia", che era stata segnalata per COVID-19, mentre i percorsi correlati al ciclo cellulare sono stati sottoregolati (Fig. 3i ). Questi risultati hanno supportato l'idea che la vaccinazione imitasse un'infezione 6 , 7 , 8 , 9 , 10 , 11, 12 .
I cambiamenti dell'espressione genica specifici del sottotipo di cellula immunitaria in primo piano rispecchiavano le alterazioni del laboratorio clinico
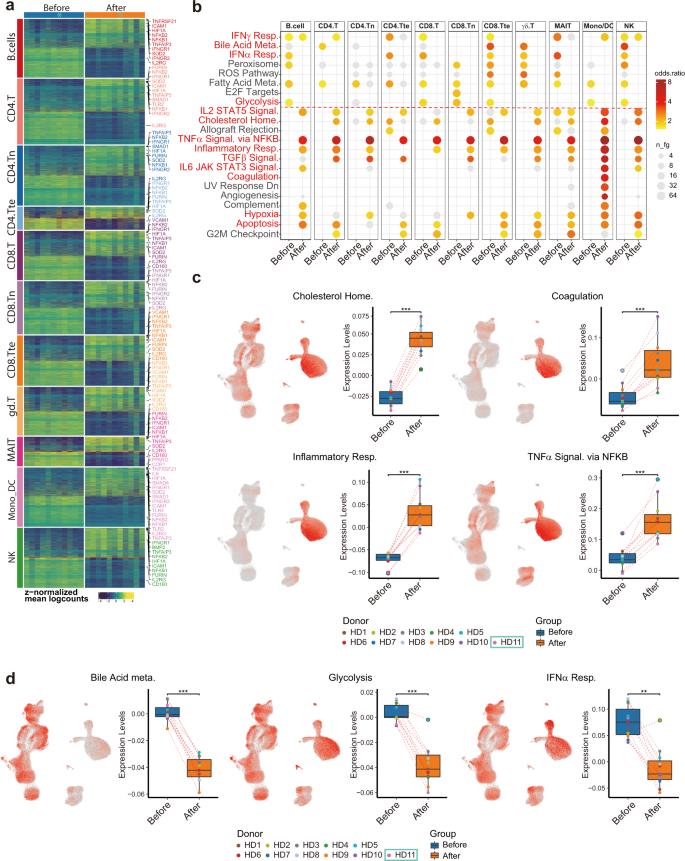
Prima della delucidazione dell'eterogeneità funzionale e dei cambiamenti dell'espressione genica specifici del tipo cellulare tra i campioni prima e dopo la vaccinazione, abbiamo raggruppato le cellule in 11 tipi principali: (1) cellule CD4 + T allo stato ingenuo , (2) CD8 allo stato ingenuo + cellule T, (3) CD4 + cellule T helper (inclusi CD4.T, CD4.Treg e CD4.Tprolif), (4) CD8 + cellule T citotossiche (inclusi CD8.T, CD8B.T e CD8.Tprolif ), (5) MAIT, (6) cellule γδ-T, (7) cellule NK (incluse NK, NK proliferative), (8) cellule B/plasmablast (incluse cellule B e plasmablasti), (9) monociti/cellule dendritiche (compresi mono classico, mono intermedio, mono non classico, DC1 mieloide1, DC2 mieloide e DC plasmacitoide), (10) CD4 + cellule T effettrici terminali e (11) CD8+ cellule T effettrici terminali. A seguito di undici principali categorizzazioni di tipi di cellule, abbiamo eseguito confronti a livello di campione aggregando l'espressione genica tra i principali tipi di cellule all'interno di ciascun donatore e quindi eseguita un'analisi dell'espressione differenziale utilizzando moscato 26 . Abbiamo identificato geni espressi in modo differenziale (DEG) tra tutti i principali tipi di cellule (Fig. 4a e Tabella supplementare S10 ) e condotto l'analisi funzionale del gene (Fig. 4b). Facendo eco ai risultati delle misurazioni cliniche, i geni correlati a "omeostasi del colesterolo", "coagulazione" e "risposta infiammatoria" (CXCL8, CD14, IL6 e TNFRSF1B), "segnalazione del TNFα tramite NF-κB" (NFKB1, NFKB2, NFKBIE, TNFAIP3 , e TNFSF9) e "ipossia" (HIF1A) sono stati sovraregolati. Inoltre, anche i geni correlati a "segnalazione TGFβ", "segnalazione IL2-STAT5" (IFNGR1, MAPKAPK2 e CASP3) e "segnalazione IL6-JAK-STAT3" (Fig. 4c ). Per visualizzare quali tipi di cellule sono stati arricchiti per quelle firme, abbiamo eseguito il punteggio del modulo genico e visualizzato i punteggi sulle coordinate UMAP e sui box plot raggruppati (Fig. 4c e tabella supplementare S11). È interessante notare che i geni della "risposta infiammatoria" erano altamente espressi nei monociti e dopo la vaccinazione aumentavano ulteriormente (Fig. 4c ), suggerendo che i monociti erano uno dei principali tipi di cellule che partecipavano alle risposte infiammatorie dopo la vaccinazione. Al contrario, i geni relativi alla "glicolisi", al "metabolismo degli acidi biliari" e alla "risposta all'interferone di tipo I (IFN-α/β)" sono stati sottoregolati, in linea con i nostri dati clinici e la fisiopatologia di COVID-19 13 (Fig. 4d ).
a 11 principali DEG specifici del tipo di cellula immunitaria identificati da dati pseudo-bulk prodotti da combinazioni di campioni prima e dopo la vaccinazione. Sono stati inclusi i geni con logFC > 0,5 e regolare P < 0,05. b L'analisi della sovrarappresentazione dei set di geni HALLMARK da MSigDB tra 11 principali tipi di cellule ha dimostrato cambiamenti comuni nei set di geni che rappresentano stati immunologici alterati prima e dopo la vaccinazione. c , d Visualizzazione UMAP colorata dai punteggi di espressione medi (livelli) basati sul percorso di arricchimento differenziale. Box plot raffigurante la distribuzione del punteggio di espressione prima e dopo la vaccinazione.
I cambiamenti più comuni in più sottotipi di cellule immunitarie hanno rivelato aumenti nella segnalazione NF-κB e diminuzioni nelle risposte IFN-α/β
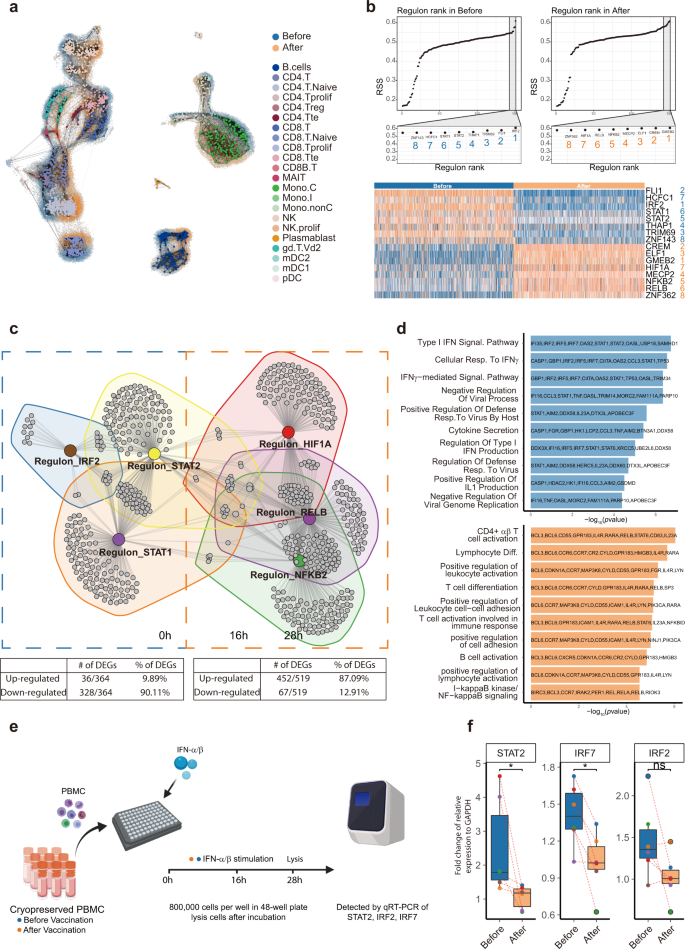
Dato che i gruppi di geni hanno cambiato drasticamente la loro espressione tra tutti i principali tipi di cellule, abbiamo ipotizzato che potrebbero esserci alcuni fattori di trascrizione che fungono da regolatori principali che portano ad alterazioni immunologiche. Per risolvere le sfide computazionali associate a un set di dati così grande, abbiamo utilizzato l'algoritmo MetaCell 27 per aggregare gruppi omogenei di cellule in metacelle e infine prodotto 1857 metacellule (893 prima e 964 dopo la vaccinazione) per rappresentare l'intera struttura del scRNA-seq dati (Fig. 5a ). Tali metacelle sono state quindi applicate a "inferenza e clustering di reti regolatorie a cella singola (SCENIC)" 28 , 29costruire le reti di regolazione genica. Il flusso di lavoro ha prodotto un elenco di 157 "regulons", che includevano i fattori di trascrizione e i loro obiettivi diretti. Le attività dei regulon sono state valutate utilizzando AUCell per accedere all'arricchimento medio di tutti i geni appartenenti a ciascun regulon in ciascuna metacellula, nonché all'arricchimento medio del gene del regulon in tutte le 893 metacellule prima della vaccinazione e 964 metacellule dopo la vaccinazione. Dopo la vaccinazione sono stati identificati otto regulons sovraregolati (più attivi) di prima classe e otto regulons downregolati (Fig. 5b ). Abbiamo selezionato 3 + 3 tipici regulons per costruire una rete regolatoria come presentato in Fig. 5c (Tabella supplementare S12). La rete ha mostrato due gruppi distinti, uno era costituito da IRF2, STAT1 e STAT2, che erano stati sottoregolati dopo la vaccinazione e l'altro conteneva RELB, NFKB2 e HIF1A, che erano stati sovraregolati dopo l'inoculazione. I termini GO della rete sovraregolata sono principalmente correlati alla differenziazione dei linfociti, all'attivazione e alla "Formazione del centro germinale", che ha suggerito che le cellule T e B sono state attivate dopo la vaccinazione. Inoltre, anche il segnale NF-kB era elevato dopo la vaccinazione. La rete sottoregolata è stata arricchita per molti percorsi correlati agli interferoni e per la secrezione di citochine (Fig. 5d e tabella supplementare S13). Questo suggerisce che la vaccinazione potrebbe inibire l'interferone risposte del sistema immunitario periferico, riducendo le attività di regulons STAT1, stat2, e IRF2, che si pensava di essere padrone fattori di trascrizione di tipo I e III guida interferone segnalazione 30 , 31 .
a Visualizzazione per le metacellule "similarità-struttura-associante" sui dati scRNA-seq originali. Le metacelle sono state codificate a colori in base alle loro annotazioni sul tipo di cellula. I dati scRNA-seq originali erano codificati a colori "blu" e "arancione" per rappresentare rispettivamente i campioni "prima" e "dopo" la vaccinazione. b Riquadri in alto: rango dei regulons nei campioni prima (a sinistra) e dopo (a destra) la vaccinazione, in base al Regulon Specificity Score (RSS). Pannelli in basso: mappa termica delle attività di regulon di primo livello prima (blu) e dopo (arancione) la vaccinazione in base ai punteggi AUCell. I nomi dei regulons sono il colore (blu/arancione) e il numero codificato (1-8). CRete di regulons e loro geni bersaglio. La tabella seguente indica la proporzione di geni all'interno dei regulons che sono stati up- o down-regolati dopo la vaccinazione. d Annotazione funzionale del gene e geni correlati prima (blu) e dopo (arancione) la vaccinazione. e Panoramica schematica dell'esperimento. f Dopo il trattamento con IFN-α/β, le PBMC dei volontari dopo la vaccinazione avevano una ridotta espressione dei geni associati alle risposte all'interferone di tipo I rispetto a quelle prima della vaccinazione. È stato utilizzato il test Wilcoxon appaiato. * P ≤ 0,05, n = 6.
Per confermare l'inibizione indotta dalla vaccinazione delle risposte all'interferone rivelata da scRNA-seq, abbiamo stimolato PBMC da individui vaccinati prima e 28 giorni dopo la vaccinazione con IFN-α/β. Dopo 16 ore di coltura e 12 ore di stimolazione, abbiamo utilizzato RT-qPCR per misurare l'espressione relativa dei regolatori principali IRF2, IRF7 e STAT2. STAT2 e IRF7 sono stati significativamente downregolati dopo la vaccinazione, tuttavia IRF2 ha mostrato una tendenza alla downregulation (Fig. 5e, f ). Le analisi del regulon hanno indicato che gli stati del sistema immunitario periferico dopo la vaccinazione avevano una ridotta risposta all'interferone di tipo I, indicativo di attenuate capacità antivirali generali almeno 28 giorni dopo la prima inoculazione.
Risposte infiammatorie indotte dalla vaccinazione nei monociti
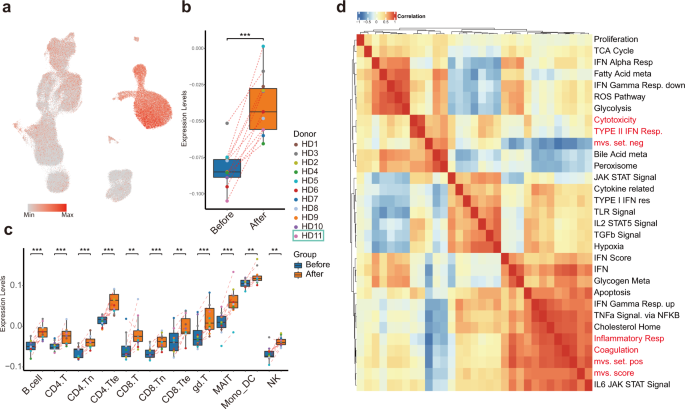
Recenti studi hanno descritto ospitanti conservato firme risposta immunitaria alle infezioni virali respiratorie, vale a dire il Meta-Virus Signature (MVS), che è anche conservata in SARS-CoV-2 infezione 32 , 33 . Punteggi MVS più alti sono associati all'infezione 32 , 33 . In tutto, 380 (158 positivamente e 222 negativamente hanno contribuito ai punteggi MVS) su 396 (161 positivamente e 235 negativamente contribuito) geni selezionati per la misurazione MVS sono stati rilevati nel nostro set di dati. Per studiare le risposte immunitarie dell'ospite dopo la vaccinazione con SARS-CoV-2 inattivato, abbiamo separato i set di geni positivi e negativi e calcolato i punteggi MVS (Fig. 6a ). I punteggi MVS erano sostanzialmente più alti dopo la vaccinazione (Fig. 6b, c), suggerendo che la vaccinazione imitava un'infezione. È interessante notare che il set di geni MVS positivo era prevalentemente espresso nei monociti, mentre il set negativo nei linfociti, indicando che diverse risposte immunitarie specifiche per tipo di cellula avrebbero avuto luogo dopo la vaccinazione (Figura complementare S3a, b ).
una visualizzazione UMAP colorata dai punteggi MVS. b I punteggi MVS in campioni pseudo-bulk che combinano tutti i tipi di cellule hanno mostrato una sovraregolazione dopo la vaccinazione. c Box plot che descrivono la distribuzione del punteggio tra 11 principali tipi di cellule immunitarie prima e dopo la vaccinazione. d Heatmap di correlazione tra punteggi MVS e percorsi arricchiti di geni differenzialmente espressi prima e dopo la vaccinazione.
Per indagare quali percorsi erano associati al set di geni MVS-positivo e al set di geni MVS-negativo, abbiamo calcolato la correlazione di Spearman tra i punteggi dei set di geni MVS e i percorsi differenzialmente arricchiti precedentemente identificati utilizzando i nostri dati scRNA-seq (Fig. 6d ). Il percorso più altamente correlato con il punteggio MVS e il set MVS-positivo era "Segnalazione della risposta infiammatoria", che è stata sorprendentemente sovraregolata nei monociti dopo la vaccinazione, insieme a CD14, FPR1, C5AR1, NAMPT, NLRP3, CDKN1A e IFNGR2. Considerando che il set MVS-negativo era ben correlato con la "firma di citotossicità", rappresentata dall'espressione di NKG7, CCL4, CST7, PRF1, GZMA, GZMB, IFNG e CCL3, significativamente diminuita in molti sottotipi di cellule T ma non nelle cellule NK dopo la vaccinazione (supplemento Fig. S3c ).
Discussione
Questa è un'indagine completa sui cambiamenti fisiopatologici, comprese le alterazioni immunologiche dettagliate nelle persone dopo la vaccinazione COVID-19. I risultati hanno indicato che la vaccinazione, oltre a stimolare la generazione di anticorpi neutralizzanti, ha anche influenzato vari indicatori di salute inclusi quelli relativi a diabete, disfunzione renale, metabolismo del colesterolo, problemi di coagulazione, squilibrio elettrolitico, come se i volontari avessero avuto un'infezione. scRNA-seq di PBMC da volontari prima e dopo la vaccinazione ha rivelato cambiamenti drammatici nell'espressione genica delle cellule immunitarie, non solo echeggiando alcune delle misure cliniche di laboratorio, ma anche indicative di un aumento delle risposte infiammatorie correlate a NF-κB, che si sono verificate principalmente nei monociti classici. La vaccinazione ha anche aumentato il contenuto dei monociti classici. Inoltre, il set di geni che contribuisce positivamente ai punteggi MVS, noto anche per essere associato allo sviluppo di sintomi gravi, era altamente espresso nei monociti. Le risposte all'interferone di tipo I (IFN-α/β), presumibilmente benefiche contro il COVID-19, sono state sottoregolate dopo la vaccinazione. Inoltre, i geni MVS negativi erano altamente espressi nei linfociti (cellule T, B e NK), ma mostravano un'espressione ridotta dopo la vaccinazione. Insieme, questi dati hanno suggerito che dopo la vaccinazione, almeno entro il 28° giorno, oltre alla generazione di anticorpi neutralizzanti, il sistema immunitario delle persone, compresi quelli dei linfociti e dei monociti, era forse in uno stato più vulnerabile. presumibilmente benefici contro il COVID-19, sono stati sottoregolati dopo la vaccinazione. Inoltre, i geni MVS negativi erano altamente espressi nei linfociti (cellule T, B e NK), ma mostravano un'espressione ridotta dopo la vaccinazione. Insieme, questi dati hanno suggerito che dopo la vaccinazione, almeno entro il 28° giorno, oltre alla generazione di anticorpi neutralizzanti, il sistema immunitario delle persone, compresi quelli dei linfociti e dei monociti, era forse in uno stato più vulnerabile. presumibilmente benefici contro il COVID-19, sono stati sottoregolati dopo la vaccinazione. Inoltre, i geni MVS negativi erano altamente espressi nei linfociti (cellule T, B e NK), ma mostravano un'espressione ridotta dopo la vaccinazione. Insieme, questi dati hanno suggerito che dopo la vaccinazione, almeno entro il 28° giorno, oltre alla generazione di anticorpi neutralizzanti, il sistema immunitario delle persone, compresi quelli dei linfociti e dei monociti, era forse in uno stato più vulnerabile.
È interessante notare che i nostri dati preliminari hanno dimostrato che se abbiamo pre-incubato RBD di SARS-CoV-2 con i PBMC (da volontari prima e dopo la vaccinazione) e quindi abbiamo trattato le cellule con IFN-α/β, le risposte all'interferone di tipo I sono state effettivamente migliorate in PBMC dopo la vaccinazione, suggerendo che forse la vaccinazione, mentre riduceva la capacità antivirale generale di una persona, migliorava la funzione immunitaria adattativa specificamente verso SARS-CoV-2 (Figura complementare S4a ). D'altra parte, confrontando i PBMC prima della vaccinazione, il pre-trattamento di SARS-CoV-2 S-RBD sembrava ridurre le risposte all'interferone di tipo I ( P <0.05, IRF2, IRF7, STAT2) (Figura complementare S4b), suggerendo che la prima esposizione del peptide virale causerebbe effettivamente una riduzione delle risposte all'interferone di tipo I nelle PBMC. Questi dati in vitro hanno ben supportato i risultati di scRNA-seq.
Vale la pena ricordare che un individuo nella coorte A che era in terapia con antibiotici, non aveva una ridotta espressione genica legata alle risposte dell'interferone di tipo I, e questo individuo aveva anche il più alto titolo anticorpale neutralizzante all'interno della coorte. Abbiamo inoltre calcolato il coefficiente di correlazione di Pearson tra i titoli anticorpali neutralizzanti e le risposte infiammatorie misurate dall'espressione genica media dei geni associati alla segnalazione del TNFα tramite NF-κB e le risposte dell'interferone-α (interferone di tipo I). I risultati sono stati 0,32 e 0,39 con P > 0,05 (Figura supplementare S4c), rispettivamente, suggerendo cambiamenti della risposta immunitaria e protezione immunitaria adattativa del vaccino non sembrano essere altamente correlati. Resta da determinare se gli antibiotici possono influenzare l'efficacia del vaccino. È anche piuttosto interessante che mentre le coorti A e B avevano diversi profili di produzione di anticorpi anti-SARS-CoV-2, i loro risultati scRNA-seq di PBMC erano drasticamente simili, inclusi i dati scRNA-seq delle cellule B (Figura complementare S5a-c). Va notato che dopo la vaccinazione, la maggior parte dei linfociti B responsivi, in particolare quelli che producono anticorpi maturi anti-COVID-19 (IgG), comprese le cellule B della memoria, dovrebbero essere localizzati principalmente nei tessuti linfatici periferici come i linfonodi e la milza, mentre solo poche cellule B mature esisterebbero in circolazione. Pertanto, la popolazione di cellule B nelle preparazioni di PBMC potrebbe non riflettere l'intero spettro dell'immunità umorale.
Le analisi presentate in questo studio, in particolare, scRNA-seq di PBMC non erano state eseguite per precedenti valutazioni del vaccino, indipendentemente dal fatto che i cambiamenti nei geni correlati alla funzione del sistema immunitario fossero specifici per COVID-19 o potessero essere generalmente applicati ad altri vaccini o altri tipi dei vaccini COVID-19 è rimasto da determinare. Tuttavia, questi tipi di analisi dettagliate dovrebbero essere complessivamente vantaggiose per lo sviluppo e le applicazioni dei vaccini. Il nostro studio postula che sia imperativo considerare il potenziale impatto a lungo termine della vaccinazione su determinate condizioni mediche 34 o sulla salute umana in generale.
Materiali e metodi
Partecipanti, raccolta dati clinici e procedure
Volontari adulti sani sono stati reclutati nel programma. Tutti i soggetti sono stati sottoposti a un esame fisico e hanno completato un questionario da medici qualificati. Nello studio sono stati arruolati adulti sani di età compresa tra 18 e 60 anni, con temperatura ascellare ≤ 37,0 ° C, negativi al test dell'acido nucleico SARS-CoV-2 e disposti a completare tutti i processi di studio programmati. Sono state escluse le persone con epilessia, malattie cerebrali o mentali, storia di allergie, malattie croniche maggiori incontrollate e risultati anormali clinicamente significativi su biochimica, test ematologici. Sono state escluse anche le donne in gravidanza o allattamento. Questo studio è stato approvato dal Comitato Etico dello Shanghai East Hospital in conformità con i principi della Dichiarazione di Helsinki (No.2020 (096)). I consensi informati scritti sono stati ottenuti da tutti i partecipanti prima dell'iscrizione.
Un totale di 11 partecipanti sono stati arruolati e vaccinati per valutare la sicurezza clinica e i cambiamenti dinamici nel sistema immunitario. Tra questi, cinque partecipanti (coorte A) sono stati vaccinati con una dose di 4 μg di vaccino SARS-CoV-2 inattivato (cellule Vero) nei giorni 1 e 14 e sei partecipanti (coorte B) hanno ricevuto una dose di 4 μg del vaccino nei giorni 1 e 28. Il vaccino SARS-CoV-2 inattivato (Vero Cell) (China Biotechnology Group Corporation) è stato somministrato per via intramuscolare nel deltoide. Tutti i vaccini sono stati approvati dal National Institutes for Food and Drug Control of China.
Test di sicurezza di laboratorio inclusi indici correlati alle infezioni (proteina C-reattiva, proteina amiloide A sierica), parametri ematologici (conta dei globuli bianchi, conta dei neutrofili, conta dei linfociti, conta dei monociti, conta dei globuli rossi, emoglobina, conta delle piastrine), funzione della coagulazione indici correlati (tempo di protrombina, tempo di tromboplastina parziale attivata/APTT, fibrinogeno, attività protrombinica/PT, rapporto internazionale normalizzato/INR), parametri correlati alla glicemia (glicemia a digiuno, HbA1c), lipidi sierici (colesterolo totale, trigliceridi, HDL -C, LDL-C), enzimi correlati alla funzione cardiaca (creatinina chinasi, CK-MB), elettroliti (potassio, sodio, cloruro, bicarbonato, calcio totale, magnesio), biomarcatori correlati alla funzione epatica (p. es., albumina, alanina aminotransferasi /ALT, aspartato aminotransferasi/AST, bilirubina totale, ecc.),Sono stati misurati i marcatori correlati alla funzione renale (creatinina, acido urico, azoto urinario nel sangue/BUN, velocità di filtrazione glomerulare stimata/eGFR).
Test degli anticorpi COVID-19 (IgG/IgM)
Un certo numero di kit di test rapidi per anticorpi COVID-19 (IgG/IgM) disponibili in commercio tra cui "Innovita (specifico per la proteina S)", "GenBody (specifico per la proteina N)", "Livzon (proteine S + N)" e "AbKhan ( proteine S + N)” sono stati utilizzati per testare le positività anti-COVID-19 (IgM/IgG) del plasma di volontari prima e in momenti diversi dopo la vaccinazione. Il kit "AbKhan" era il più sensibile e i dati sono stati utilizzati in questo studio.
Test degli anticorpi neutralizzanti con PRNT
I campioni di siero sono stati testati ciascuno utilizzando un test di neutralizzazione della riduzione della placca (PRNT) per SARS-CoV-2 (2019-nCoV-WIV04) nel laboratorio BSL-3. In breve, i sieri sono stati inattivati al calore a 56 °C per 30 minuti e diluiti a 1:50, seguiti da tre diluizioni seriali (1:50, 1:150, 1:450, 1:1350, 1:4050 e 1: 12,150). I sieri sono stati quindi miscelati con 100 PFU di virus e incubati a 37 ° C per 1 h. Le miscele di diluizione virus-siero e il controllo del virus sono stati quindi inoculati in monostrati di cellule Vero E6 in piastre da 24 pozzetti per 1 ora prima di aggiungere un mezzo di sovrapposizione comprendente 1,5% di metilcellulosa a 37 ° C per 4-5 giorni per consentire lo sviluppo della placca. Quindi le piastre sono state fissate e colorate con cristalvioletto al 2% in metanolo al 30% per 30 minuti a temperatura ambiente e le piastre sono state contate e misurate manualmente.
Preparazione di sospensioni unicellulari, preparazione di librerie di RNA unicellulari e sequenziamento
I PBMC sono stati isolati da sangue venoso eparinizzato da volontari sani utilizzando un terreno Ficoll-Paque TM PLUS (GE Healthcare Inc.) secondo il metodo di centrifugazione a gradiente di densità standard fornito dal produttore. I PBMC sono stati congelati in un mezzo di congelamento (70% RPMI-1640, 20% FBS e 10% DMSO) e conservati in azoto liquido fino all'uso. La cattura di una singola cella e la costruzione della libreria sono state eseguite utilizzando il kit Chromium Single Cell 5′ Library & Gel Bead (10× Genomics) secondo le istruzioni del produttore. Le librerie sono state sequenziate utilizzando la piattaforma Novaseq 6000 (Illumina).
Analisi e statistiche dei dati scRNA-seq
I dati di sequenziamento di singole cellule sono stati allineati e quantificati utilizzando kallisto/bustools (KB, v0.25.0) 35 rispetto al genoma di riferimento umano GRCh38 scaricato dal sito Web ufficiale di 10× Genomics. I conteggi preliminari sono stati quindi utilizzati per le analisi a valle. Abbiamo creato una pipeline per elaborare i dati. In breve, le cellule con meno di 200 geni sono state filtrate, i conteggi logaritmici normalizzati e la selezione dei primi 3000 geni altamente variabili (HVG) sono stati eseguiti da Scanpy 36 .
Abbiamo escluso geni specifici da HVG inclusi geni mitocondriali, geni delle immunoglobuline e geni collegati a modelli trascrizionali scarsamente supportati (annotati con il prefisso "Rp-"). Quindi è stata eseguita l'analisi dei componenti principali (PCA) utilizzando gli HVG e l'algoritmo Harmony è stato utilizzato per rimuovere gli effetti batch 25 . Abbiamo utilizzato l'approccio PARC per identificare i cluster 37 e le caratteristiche selezionate mediante la funzione "FeatureSelectionByEnrichment" dall'algoritmo cytograph2 38 , seguito da un altro ciclo di PCA, Harmony e PARC. Successivamente, abbiamo calcolato K vicini più prossimi in un grafico KNN, eseguito l'approssimazione e la proiezione di varietà uniformi (UMAP) di Pegasuspy 39 e identificato i cluster di PARC. Inoltre, abbiamo applicato Scrublet 40 per identificare potenziali doppietti.
Il controllo di qualità è stato applicato ai cluster in base all'output del primo round della pipeline:
- 1.
I cluster con più del 20% di cellule di cui un punteggio di doppietto > 0,4 sono stati definiti come cluster di doppietti.
- 2.
I cluster con più del 20% di cellule che avevano > 20% delle loro trascrizioni mappate ai geni mitocondriali sono stati definiti come cluster di bassa qualità.
- 3.
I cluster con più del 20% di cellule che avevano < 0,05% delle loro trascrizioni mappate ai geni mitocondriali sono stati definiti come nuclei.
- 4.
Espressione mediana di PPBP, PF4, HBB, HBA2 > 0, che indica eritrociti e piastrine.
- 5.
Meno di 50 cellule.
- 6.
Numeri di geni rilevati < 1000.
- 7.
Rapporto tra la media delle UMI totali e la media dei geni rilevati < 2.
- 8.
Scrublet ha identificato doppietti.
- 9.
Utilizzo di DBSCAN 41 per rimuovere i valori anomali.
Dopo aver rimosso le cellule di bassa qualità, abbiamo annotato le cellule dal riconoscimento cella singola di tipi di cellule (Singler) algoritmo, riferendosi a Monaco set di dati del sistema immunitario 42 .
Le cellule qualificate sono state sottoposte ad analisi a valle. Allo stesso modo, eseguiamo nuovamente la pipeline per identificare i principali tipi di cellule tra cui le cellule T (CD3D, CD3E, CD3G, CD40LG, CD8A, CD8B), le cellule B (MS4A1, CD79A, CD79B), le cellule NK (GNLY, NKG7, TYROBP, NCAM1), e monociti (CST3, LYZ). Inoltre, eseguiamo la pipeline su ciascun tipo di cellule, rispettivamente, e sottotipi ulteriormente identificati in base ai tipi di cellule identificati da SingleR e marcatori ben caratterizzati (Fig. 3b ).
Confronto della proporzione delle cellule immunitarie
Per i campioni da PBMC, abbiamo calcolato le proporzioni delle cellule immunitarie per ciascun tipo di cellula principale e sottotipi sottostanti. Per ogni campione, la proporzione del tipo di cellula è stata calcolata dal numero di cellule in un certo tipo di cellula diviso per il numero totale di cellule. Per identificare i cambiamenti nelle proporzioni cellulari tra campioni in gruppi diversi, abbiamo eseguito un test di Wilcoxon sulle proporzioni di ciascun tipo di cellula principale e sui sottotipi di cellule tra gruppi diversi (Figura supplementare S2 ). Solo quei tipi di cellule con differenze statisticamente significative ( P < 0,05) nelle proporzioni sono mostrati in Fig. 3e .
Analisi dell'espressione differenziale, analisi della sovrarappresentazione dei set di geni e moduli per la firma del punteggio
Per indagare sulle alterazioni delle caratteristiche immunologiche, abbiamo identificato i DEG mediante l'algoritmo muscat 26 con parametri predefiniti. In breve, abbiamo prima sommato i dati, sommando gli UMI tra le cellule per ciascun donatore sano, per produrre un profilo UMI in stile RNA-seq di massa per ciascun campione. Successivamente, i conteggi aggregati sono stati caricati sulla funzione pbDS per identificare i DEG e le mappe di calore sono state tracciate dalla funzione pbHeatmap. L'analisi della sovrarappresentazione del set di geni dei DEG (logFC > 0,5 e P aggiustato < 0,05) è stata eseguita utilizzando il test esatto di Fisher unilaterale (come implementato nel pacchetto R "gsfisher") con il gene "HALLMARK", "KEGG" e "REACTOME" set derivati da MSigDB. Insiemi di geni con P < 0,05 sono stati considerati significativi. I punteggi del modulo Signature sono stati calcolati tramite la funzione "AddModuleScore", con impostazioni predefinite in Seurat. In breve, per ciascuna cellula, il punteggio è stato definito come l'espressione media dell'elenco di geni di firma sottraendo l'espressione media dell'elenco di geni di controllo corrispondente 43 . Gli elenchi di geni utilizzati per l'analisi sono forniti nella tabella supplementare S11 .
Analisi metacella
Abbiamo utilizzato il pacchetto R “MetaCell” 27 per analizzare i dati. Abbiamo rimosso specifici geni mitocondriali, geni delle immunoglobuline e geni collegati a modelli trascrizionali scarsamente supportati (annotati con il prefisso "Rp-"). Abbiamo quindi filtrato le cellule con meno di 500 UMI. Le caratteristiche del gene sono state selezionate utilizzando il parametro Tvm = 0,08 e un conteggio totale minimo di UMI > 100. Successivamente abbiamo eseguito il clustering gerarchico della matrice di correlazione tra quei geni (filtro di geni con bassa copertura e correlazione di calcolo utilizzando una matrice UMI sottocampionata) e selezionato cluster di geni contenenti geni di ancoraggio. Abbiamo usato K = 100 e 500 iterazioni bootstrap e parametri altrimenti standard. Le metacelle sono state annotate dai tipi di cellule più abbondanti che compongono ciascuna metacella.
Analisi della rete di regolazione genica
Per l'identificazione e il punteggio dell'attività del regulon, abbiamo impiegato pySCENIC 28 , 29flusso di lavoro su dati metacellule log normalizzati per determinare set di geni co-espressi. Abbiamo collegato i bersagli diretti ai loro corrispondenti fattori di trascrizione utilizzando i database RcisTarget (v1.2.1) e mantenuto i putativi geni a valle con motivi di DNA arricchiti a 10 kb o 500 bp dal sito di inizio della trascrizione (punteggio di arricchimento normalizzato > 3). Infine, abbiamo utilizzato la funzione AUCell per valutare l'attività di ciascun regulon tra le cellule nel set di dati, che è stata calcolata come la somma dei geni espressi per regulon e ha prodotto matrici di attività binarie basate su cutoff regolati manualmente dopo aver ispezionato le distribuzioni dei punteggi AUC. I punteggi di specificità di Regulon (RSS) sono stati calcolati dalla funzione "regulon_specificity_scores" dall'algoritmo pySCENIC con parametri predefiniti.
Analisi della risposta IFN-α/β delle PBMC
Le PBMC sono state isolate dal sangue eparinizzato mediante Ficoll-Hypaque a 400 × g per 30 min. I PBMC (1 × 10 6 ml -1 ) dei donatori prima e dopo la vaccinazione sono stati quindi seminati in piastre di coltura da 48 pozzetti con RPMI-1640 contenente il 5% di siero sostitutivo e 0,032% di eparina. Il giorno successivo, il terreno è stato scambiato e le cellule sono state trattate con 100 ng/ml di IFN-α e 10 ng/ml di IFN-β per 12 ore. Alcune cellule sono state pretrattate con 250 ng/ml di RBD per 16 ore, seguite da trattamento con IFN-α/β per 12 ore. Dopo il lavaggio e l'estrazione dell'RNA totale, è stata eseguita la PCR quantitativa in tempo reale per rilevare l'espressione dei geni associati alla risposta dell'interferone di tipo I. Le variazioni di piega relative a GAPDH sono state calcolate di 2 -ΔΔCted espresso come mezzo ± SEM. Le differenze tra i gruppi sono state valutate utilizzando il test t di Student per appaiati e considerate significative quando P <0.05.
analisi statistica
I dati clinici sono stati riassunti utilizzando la media (deviazione standard), la mediana (Q1, Q3) o il numero (percentuale), quando appropriato. Il test dei ranghi con segno di Wilcoxon è stato utilizzato per confrontare le mediane appaiate nel tempo per le caratteristiche di laboratorio. Inoltre, il test somma-rank di Wilcoxon è stato utilizzato per confrontare le variazioni mediane rispetto al basale tra le coorti A e B. Abbiamo classificato gli eventi avversi in base alla scala pubblicata dalla China National Medical Products Administration ( https://www.nmpa.gov. cn/xxgk/ggtg/qtggtg/20191231111901460.html ) e il giudizio sui risultati dei test di laboratorio si è basato sull'intervallo di valori di riferimento della popolazione locale. Tutti i test statistici erano a due code. La significatività statistica è stata definita come P 0,05. Le analisi statistiche sono state eseguite utilizzando SAS v9.4 (SAS Institute Inc., Cary, NC, USA).
Disponibilità dei dati
I numeri di accesso per i dati grezzi di sequenziamento e i dati elaborati in questo documento sono Genome Sequence Archive nel BIG Data Center (GSA, Beijing Institute of Genomics, Chinese Academy of Sciences): HRA001150.
Commenti
Posta un commento